Compuestos ternarios: OXOSALES
📐📏 Oxosales: Nomenclatura y Formuleo📚🔍
En esta nueva explicación sobre la nomenclatura y formuleo, nos vamos a concentrar en las OXOSALES. Veremos este grupo de compuestos ternarios en detalle para luego practicar lo aprendido con ejercicios.
¿A qué llamamos oxosal y cuáles son sus características?
Una OXOSAL es un compuesto ternario IÓNICO, es decir, que es la interacción NO covalente entre un anión y un catión. En este tipo de compuestos ternarios, el catión es un METAL y el anión es un complejo derivado de un oxoácido.Teniendo en cuenta la estrcutura de un oxoácido:
HxNyOz
Se denomina oxoanión, a la especie que resulta de la separación del catión H+ del complejo NyOz que es, es el anión. Esta especie recibe el nombre de OXO-anión debido a que el oxígeno es un componente obligado de este complejo, y anión porque la carga neta de este complejo es negativa:
NyOz-
En solución acuosa, el oxoanión interactuará con un catión metálico dando lugar a la formación de una OXOSAL u OXISAL (Figura 1). En el siguiente ejemplo podemos ver que el hierro, Fe, (un metal electropositivo) tenderá a interactuar con el oxoanión de azufre, dando lugar a una oxosal:
Figura 1: Oxosal de Hierro y Sulfato.
Las oxosales pueden formarse a partir de disociaciones parciales de los oxoácidos
Cuando el anión de un oxoácido no pierde todos los hidrógenos, da lugar a oxoaniones ácidos. Se los denomina así debido a que el anión ahroa está conformado por un H, un No metal y el O (HXOn-). Para dar un ejemplo, podemos ver el caso del ácido fosfórico o ácido ortofosfórico: H3PO4.
Esta molécula es un oxoácido, y no necesariamente se desprenderá de todos los hidrógenos. La permanencia de algunos hidrógenos en su estructura se debe a la relativamente baja fuerza ácida característica de este compuesto. Es decir, no se solvata completamente. Veamos como se presenta la fpormula a continuación:
Figura 2: El Oxoácido pierde 2 H+ de los 3 que conforma su estructura. Esto da lugar a la formación de un oxoanión con un hidrógeno.
Este oxoanión puede interactuar con un catión metálico dando lugar a lo que denominamos: SAL ÁCIDA.
Figura 3: Ejemplo de una sal ácida de Níquel
Sin embargo, este es un compuesto cuaternario, cuya explicación la encontrarás haciendo click acá.
OXOSALES TERNARIAS. Estructura general de la fórmula:
Como regla general, en la fórmula de todos estos compuestos iónicos aparece en primer lugar el catión y a continuación, la parte aniónica:
Donde:
M= metal (catión)
N= es el no metal diferente del oxígeno
O= oxígeno
NOMENCLATURA DE LAS SALES TERNARIAS
Para nombrar oxosales por esta nomenclatura, debemos tener en cuenta los sufijos que corresponden a los números de oxidación menor o mayor. En los compuestos que habíamos estudiado hasta ahora eran: OSO e ICO. Sin embargo, para las oxosales, estos sufijos van a cambiar a ITO y ATO respectivamente.
En esta nomenclatura, se antepone el nombre del No metal (diferente de oxígeno) con la terminación ITO o ATO y, en el caso que el no metal tenga mas de 2 números de oxidación, será:
No metal ____ de Metal
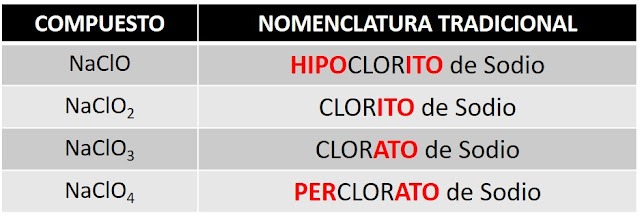
En este caso el cloro actúa en cada ocasión con uno de sus cuatro (4) números de oxidación. Esto nos obliga a jugar con los prefijos y sufijos para denominar cada compuesto iónico de forma correcta.
 NOMENCLATURA SISTEMÁTICA
NOMENCLATURA SISTEMÁTICA
Para nombrar compuestos utilizando esta nomenclatura debemos mencionar primero el ANIÓN, con el prefijo que indique la atomicidad del oxígeno, el número de oxidación del No metal en números romanos y por último se agrega "de metal" y el número de oxidación de éste en números romanos...¡veamos un ejemplo para resumir esto!
En el caso que el metal actúe con más de un número de oxidación, agregamos dicho número entre paréntesis y en numeración romana:
 NOMENCLATURA DE STOCK
NOMENCLATURA DE STOCK
Por último, veamos como nombrar a estos compuestos mediante la nomenclatura de Stock. En este caso debemos nombrar al complejo del oxoanión al igual que en la nomenclatura tradicional, utilizando los prefijos y sufijos:
- PER___ATO
- ____ATO
- ____ITO
- HIPO___ITO
Por último, nombramos el metal seguido de su número de oxidación entre paréntesis y en números romanos como se muestra en la tabla:
También te puede interesar:
1. Sales binarias. Nomenclatura y formuleo.
2. Hidróxidos. Nomenclatura y formuleo.
Referencias
Soy Licenciada en Ciencias Biológicas y tengo un PhD en Química Biológica. Escribo esta página basada en mi experiencia como docente e investigadora y utilizo fuentes de información confiables para la redacción de los artículos que dejo a continuación: